۱. پیشینه اپیدمی دنگی: یک چالش رو به رشد بهداشت عمومی جهانی
تب دنگی یک بیماری ویروسی حاد منتقله از طریق پشه است که توسط ویروس دنگی (DENV) ایجاد میشود و به عنوان سریعترین بیماری آربوویروسی در سطح جهان ظهور کرده و تهدیدی اساسی برای امنیت بهداشت عمومی محسوب میشود. در طول دو دهه گذشته، میزان شیوع جهانی تب دنگی به طرز چشمگیری افزایش یافته است، به طوری که تعداد موارد گزارش شده از سال 2021 سالانه دو برابر شده است [1]. در دسامبر 2023، سازمان بهداشت جهانی (WHO) برای تقویت تلاشهای هماهنگ بینالمللی در واکنش به این بیماری، وضعیت اضطراری جهانی تب دنگی را اعلام کرد. برآوردهای اپیدمیولوژیک سازمان بهداشت جهانی نشان میدهد که تقریباً 3.9 میلیارد نفر در سراسر جهان در معرض خطر ابتلا به عفونت دنگی هستند و سالانه حدود 390 میلیون عفونت رخ میدهد که از این تعداد 96 میلیون نفر به صورت موارد بالینی آشکار ظاهر میشوند [1،2].
۲ نکات برجسته اپیدمیولوژیک
ویژگیهای اپیدمیولوژیک تب دنگی تحت تأثیر تعامل عوامل ویروسی، بومشناسی ناقل، پاسخهای ایمنی میزبان و شرایط اجتماعی-محیطی قرار دارد. درک جامع از این ویژگیها برای توسعه استراتژیهای مؤثر پیشگیری و کنترل و همچنین رویکردهای تشخیصی دقیق ضروری است.
۲.۱ بردارهای انتقال و الگوهای انتقال شهری
ویروس دنگی در درجه اول از طریق ... منتقل میشود.آئدس اجیپتی و آئدس آلبوپیکتوسپشهها. در میان این گونههای ناقل، آئدس آجیپتی به عنوان مهمترین ناقل انتقال شناخته میشود که با «سازگاری بالا با انسان» و پراکندگی گسترده در محیطهای شهری گرمسیری و نیمهگرمسیری مشخص میشود. برخلاف سایر ناقلین پشهای پاتوژنهای آربوویروسی، آئدس آجیپتی ویژگیهای اپیدمیولوژیک کلیدی زیر را نشان میدهد:
- ترجیح برای پرورش در محیطهای انسانی (مثلاً ظروف ذخیره آب، لاستیکهای اسقاطی)
- گرایش قوی به خون انسان به عنوان منبع مواد مغذی
-رفتار تغذیه در طول روز
این ویژگیها، تب دنگی را به عنوان یک بیماری معمول تعریف میکنند.«بیماریهای واگیردار شهری»با راندمان انتقال قابل توجهی در مناطق پرجمعیت افزایش یافته است. مطالعات مرتبط با سازمان بهداشت جهانی نشان داده است که در مناطق شهری با تراکم بالا، افزایش دفعات تماس پشه و انسان میتواند به طور قابل توجهی عدد تکثیر پایه (R₀) ویروس DENV را افزایش دهد و در نتیجه گسترش همهگیریها را تسریع کند [2].
۲.۲ روندهای جهانی گسترش و عوامل مؤثر
طبق گزارشهای سازمان بهداشت جهانی، تعداد جهانی موارد گزارششده تب دنگی طی دو دهه گذشته به صورت تصاعدی افزایش یافته است [1،3]. این روند صعودی در درجه اول توسط عوامل به هم پیوسته زیر هدایت میشود:
(1) تغییرات اقلیمی: افزایش دمای جهانی نه تنها محدوده جغرافیایی زیستگاههای مناسب برای پشههای ناقل را گسترش میدهد، بلکه دوره کمون بیرونی DENV را در میزبان پشه نیز کوتاه میکند و در نتیجه راندمان انتقال را افزایش میدهد. تغییرات ناشی از آب و هوا در تراکم پشهها توسط سازمان بهداشت جهانی به عنوان یک پیشبینیکننده قابل اعتماد از پویایی مکانی-زمانی شیوع تب دنگی تأیید شده است.
(2) شهرنشینی: گسترش سریع و بدون برنامهریزی شهری، زیستگاههای فراوانی برای تولید مثل پشههای ناقل ایجاد کرده است، در حالی که افزایش تراکم جمعیت، تداوم زنجیرههای انتقال DENV را تقویت کرده است.
(3) جابجایی جمعیت جهانی: سفر و تجارت بینالمللی انتقال سریع فرامرزی DENV را تسهیل کرده و انتقال از موارد وارداتی به انتقال پایدار محلی را تسهیل کرده است. دادههای نظارتی سازمان بهداشت جهانی نشان میدهد که بین سالهای 2010 تا 2021، ایالات متحده 7528 مورد تب دنگی مرتبط با سفر را گزارش کرده است که از این تعداد 3135 مورد نیاز به بستری شدن در بیمارستان داشته و 19 مورد منجر به مرگ شده است.
(4) گسترش توزیع ناقل: در سطح جهان، محدوده جغرافیایی Aedes aegypti و Aedes albopictus همچنان در حال گسترش است و پشههای Aedes به طور فزایندهای در بخشهایی از اروپا مستقر میشوند. در نتیجه، تب دنگی از یک اپیدمی سنتی منطقهای به یک تهدید جهانی برای سلامت عمومی تبدیل شده است.
۲.۳ مکانیسمهای گردش خون همزمان و عفونت مجدد چند سروتیپی
ویروس دنگی شامل چهار سروتیپ آنتیژنی متمایز (DENV-1 تا DENV-4) است. عفونت با یک سروتیپ، ایمنی محافظتی طولانیمدت در برابر آن سروتیپ خاص ایجاد میکند، اما تنها محافظت متقاطع موقت و جزئی در برابر سه سروتیپ دیگر ایجاد میکند. عموم مردم به طور کلی در برابر DENV حساس هستند و تنها زیرمجموعهای از افراد آلوده دچار بیماری بالینی میشوند [2].
در مناطق بومی، چندین سروتیپ DENV اغلب به طور همزمان در گردش هستند و در نتیجه افراد میتوانند در طول زندگی خود عفونتهای متعدد دنگی را تجربه کنند. مطالعات اپیدمیولوژیک سازمان بهداشت جهانی، گردش همزمان چند سروتیپ را به عنوان عامل اصلی شیوع دورهای دنگی شناسایی کردهاند [1].
۲.۴ عفونت ثانویه و تقویت وابسته به آنتیبادی
یک پدیده حیاتی و منحصر به فرد در اپیدمیولوژی تب دنگی است.تقویت وابسته به آنتیبادی (ADE)در طول عفونت ثانویه با سروتیپ هترولوگ DENV، آنتیبادیهای غیرخنثیکننده تولید شده در طول عفونت اولیه، ورود ویروس به مونوسیتها و ماکروفاژها را تسهیل میکنند و در نتیجه تکثیر ویروس را افزایش میدهند. این مکانیسم به طور گسترده توسط سازمان بهداشت جهانی به عنوان یک عامل بیماریزای اصلی در تب دنگی شدید، از جمله تب خونریزی دهنده دنگی و سندرم شوک دنگی شناخته شده است [1].
دادههای اپیدمیولوژیک سازمان بهداشت جهانی به طور مداوم نشان میدهند که افراد مبتلا به عفونت ثانویه دنگی در مقایسه با افراد مبتلا به عفونت اولیه، خطر ابتلا به بیماری شدید را به طور قابل توجهی بالاتر دارند - مشخصه ای که برای نظارت بر بیماری و مدیریت بالینی از اهمیت بالایی برخوردار است. توجه به این نکته مهم است که اگرچه خطر بیماری شدید در طول عفونت ثانویه افزایش مییابد، اما عفونت با هر سروتیپ DENV میتواند به طور بالقوه به دنگی شدید تبدیل شود [1].
۲.۵ تظاهرات بالینی غیر اختصاصی و خطر تشخیص اشتباه
تظاهرات بالینی تب دنگی به ویژه در مراحل اولیه بیماری، غیر اختصاصی است و اغلب با سایر عفونتهای ویروسی منتقله از طریق پشه (مانند ویروسهای چیکونگونیا و زیکا) و همچنین برخی عفونتهای تنفسی همپوشانی دارد. برآوردهای سازمان بهداشت جهانی نشان میدهد که 40 تا 80 درصد از عفونتهای DENV بدون علامت هستند [3].
تظاهرات بالینی معمول عبارتند از:
تب حاد (که به مدت ۲ تا ۷ روز ادامه دارد و ممکن است دو مرحلهای باشد)
- سردرد شدید و درد پشت چشم (درد پشت چشم)
درد عضلات و مفاصل (که معمولاً به آن «تب استخوانشکن» میگویند)
- بثورات ماکولار یا ماکولوپاپولار
- تظاهرات خونریزی خفیف (مثلاً اکیموز، خونریزی از بینی، خونریزی لثه)
تب دنگی علامتدار معمولاً به سه مرحله مجزا تقسیم میشود: مرحله تب، مرحله بحرانی و مرحله بهبودی. تقریباً کمتر از 5٪ از بیماران علامتدار به تب دنگی شدید مبتلا میشوند. به دلیل فقدان ویژگیهای بالینی خاص، تشخیص صرفاً بر اساس علائم بالینی چالشبرانگیز است، که خطر تشخیص نادرست و عدم تشخیص کافی را افزایش میدهد. سازمان بهداشت جهانی (WHO) به صراحت تأکید میکند که تشخیص بالینی به تنهایی برای اطمینان از دقت کافی نیست و تأیید آزمایشگاهی را ضروری میسازد [1].
۳ نکته کلیدی از سازمان بهداشت جهانی «آزمایش آزمایشگاهی ویروس دنگی: راهنمای موقت، آوریل ۲۰۲۵»
در آوریل ۲۰۲۵، سازمان بهداشت جهانی راهنمای موقت بهروز شدهای را در مورد آزمایشهای آزمایشگاهی برای DENV منتشر کرد که راهنمایی فنی معتبری را برای تشخیص جهانی تب دنگی ارائه میدهد. این راهنما، آخرین شواهد مربوط به آزمایشهای آزمایشگاهی تب دنگی را در زمینه وضعیت اضطراری جهانی تب دنگی ترکیب میکند و توصیههای عملی متناسب با شرایط با سطوح مختلف منابع ارائه میدهد.

۳.۱ اصول اساسی استراتژی تست
این راهنما تأکید میکند که تشخیص تب دنگی باید بر اساس مرحله بیماری، یک استراتژی آزمایش ترکیبی چند نشانگری اتخاذ کند [1]. با توجه به عدم وجود یک الگوریتم تشخیصی جهانی، استراتژیهای آزمایش باید با توجه به شرایط اپیدمیولوژیک محلی و با در نظر گرفتن عوامل کلیدی زیر تطبیق داده شوند [1]:
مرحله عفونت: تعداد روزهای پس از شروع علائم، مناسبترین روش آزمایش را تعیین میکند.
نوع نمونه: مناسب بودن خون کامل، پلاسما یا سرم برای تشخیص DENV
اپیدمیولوژی منطقهای: سروتیپهای در گردش محلی DENV و گردش همزمان سایر آربوویروسها
-خطر عفونت همزمان: در مناطقی که گردش آربوویروسها با هم همپوشانی دارد، باید آزمایش چندگانه برای تمایز بین عوامل بیماریزای مختلف در نظر گرفته شود.
۳.۲ استراتژی تست مبتنی بر مرحله
طبق دستورالعمل سازمان بهداشت جهانی، آزمایشهای آزمایشگاهی تب دنگی باید بر اساس مرحله بیماری، از بازههای زمانی مشخصی پیروی کنند [1،2]:
(1) آزمایش فاز حاد (≤7 روز پس از شروع)
آزمایش اسید نوکلئیک (آزمایش مولکولی): واکنش زنجیرهای پلیمراز رونویسی معکوس (RT-PCR) و سایر روشهای مولکولی، RNA ویروس دنوری (DENV) را با حساسیت بالا تشخیص میدهند.
آزمایش آنتیژن: تشخیص آنتیژن NS1، که ظرف ۱ تا ۳ روز پس از شروع بیماری قابل تشخیص میشود.
در طول فاز حاد، سطح ویرمی نسبتاً بالا است و آزمایش اسید نوکلئیک و آنتیژن به حساسیت بهینه میرسند.
(2) آزمایش مرحله نقاهت (≥4 روز پس از شروع بیماری)
آزمایش سرولوژیکی: آنتیبادیهای IgM معمولاً حدود روز چهارم پس از شروع بیماری قابل تشخیص میشوند.
در بیشتر موارد، آنتیبادیهای IgM به مدت ۱۴ تا ۲۰ روز باقی میمانند و در برخی موارد، ماندگاری آنها میتواند تا ۹۰ روز نیز ادامه یابد.
آزمایش IgG به دلیل احتمال واکنش متقاطع آنتیبادیها از عفونت قبلی با فلاویویروس یا واکسیناسیون، ارزش محدودی برای تشخیص تب دنگی حاد دارد.
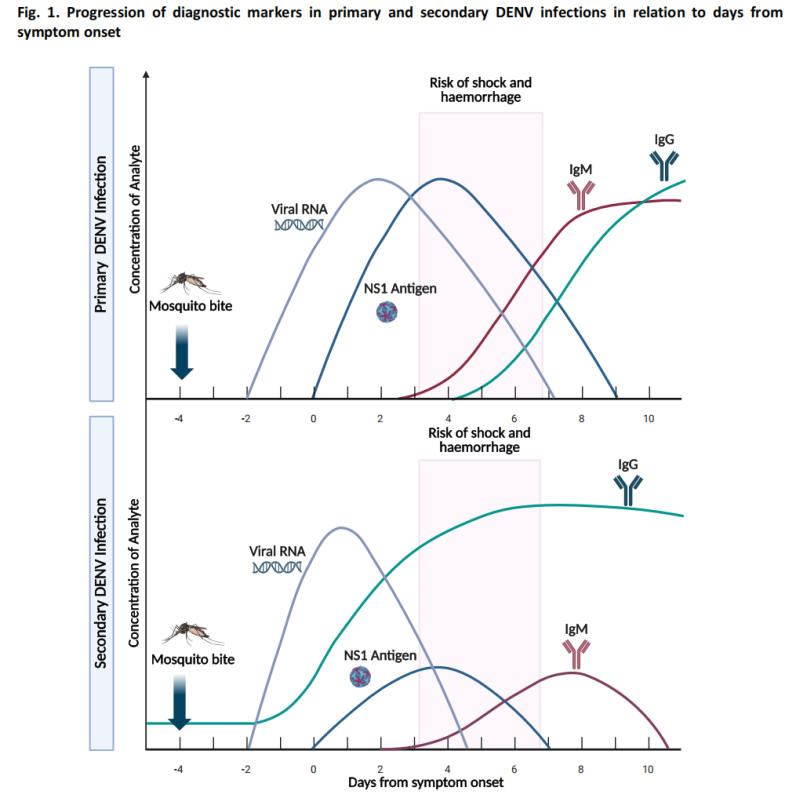
(3) الگوریتم تشخیص موارد مشکوک
این راهنما شامل یک الگوریتم تشخیصی برای موارد مشکوک به تب دنگی است که روشهای آزمایش مناسب را بر اساس روزهای پس از شروع علائم توصیه میکند: آزمایش آنتیژن NS1 و آزمایش اسید نوکلئیک رویکردهای اصلی در مرحله اولیه هستند، در حالی که آزمایش سرولوژیکی روش اصلی در مرحله بعدی است.
۳.۳ ارزیابی و انتخاب عملکرد روش آزمون
طبق گفته سازمان بهداشت جهانی، ارزیابی سیستماتیک عملکرد و سناریوهای قابل اجرا برای آزمایشهای مختلف تب دنگی به شرح زیر است:
| روش آزمایش | هدف | پنجره زمانی | سناریوی کاربرد اولیه | ملاحظات |
| آزمایش اسید نوکلئیک | RNA ویروسی | ۱-۷ روز پس از شروع | تأیید اولیه، شناسایی سروتیپ | روش استاندارد طلایی؛ نیازمند تجهیزات آزمایشگاهی تخصصی و تخصص فنی است |
| آزمایش آنتیژن NS1 | پروتئین غیرساختاری | ۱-۳ روز پس از شروع | غربالگری سریع اولیه | موجود در قالب تست تشخیص سریع (RDT)، مناسب برای محیطهای با منابع محدود |
| آزمایش آنتی بادی IgM | آنتیبادیهای اختصاصی IgM | ≥۴ روز پس از شروع | تشخیص عفونت اخیر | یک نمونه سرم تنها نشاندهنده عفونت احتمالی اخیر است؛ برای تأیید، سروکانورژن لازم است |
| آزمایش آنتی بادی IgG | آنتیبادیهای اختصاصی IgG | عفونت در دوران نقاهت/قبل از آن | بررسی اپیدمیولوژیک، ارزیابی وضعیت ایمنی | یک نمونه سرم واحد برای تشخیص تب دنگی حاد مناسب نیست |
| آزمایش ترکیبی (NS1+IgM/IgG) | آنتیژن + آنتیبادی | دوره کامل بیماری | تشخیص جامع عفونت دنگی | در حال حاضر، بهترین فرمت RDT برای تشخیص تب دنگی |
| ان جی اس | RNA ویروسی | ۱-۷ روز پس از شروع | نظارت ژنومی ویروسی | نیاز به تجهیزات تخصصی تعیین توالی و قابلیتهای تحلیل بیوانفورماتیک دارد |
۴ توصیه محصول تشخیص تب دنگی در مقیاس کلان و خرد بر اساس سناریو
برای پشتیبانی از پیشگیری و کنترل تب دنگی، Macro & Micro-Test یک مجموعه تشخیصی یکپارچه ارائه میدهد که شامل غربالگری سریع، تأیید مولکولی و نظارت ژنومی است و نیازها را در مراحل مختلف مدیریت شیوع برآورده میکند.
۴.۱ سناریوی ۱: غربالگری سریع و نظارت هدفمند
قابل استفاده در کلینیکهای تب، مراکز مراقبتهای بهداشتی اولیه، غربالگری جامعه در زمان شیوع بیماری و قرنطینه بندر/مرز.
-آزمایش سریع آنتیژن NS1 ویروس دنگی: عفونت اولیه (1 تا 3 روز پس از شروع) را با نتایج 15 دقیقهای برای تریاژ سریع تشخیص میدهد.
آزمایش آنتیبادی IgM/IgG ویروس دنگی: عفونتهای اولیه/ثانویه را برای ارزیابی خطر ابتلا به بیماری شدید تشخیص میدهد.
-آزمایش سریع ترکیبی آنتیژن NS1 ویروس دنگی + IgM/IgG: به طور همزمان آنتیژن و آنتیبادیها را برای تشخیص کامل بیماری شناسایی میکند.
آزمایش آنتیبادی IgM/IgG ویروس چیکونگونیا: تشخیص افتراقی با تب دنگی را برای شناسایی دقیق عوامل بیماریزا امکانپذیر میکند.
۴.۲ سناریو ۲: تشخیص دقیق و واکنش اضطراری
کیت تشخیص اسید نوکلئیک ویروس دنگی I/II/III/IV: 4 سروتیپ (حد تشخیص 500 کپی در میلیلیتر) را برای ردیابی شیوع بیماری تشخیص داده و از هم متمایز میکند.
کیت PCR ویروس دنگی لیوفیلیزه: قابل حمل در دمای اتاق، مناسب برای مناطق با منابع محدود و شیوع ناگهانی.
کیت PCR چندگانه Real-Time برای تشخیص تب دنگی/زیکا/چیکونگونیا: به طور همزمان ۳ آربوویروس را برای تشخیص افتراقی کارآمد در شیوعهای پیچیده شناسایی میکند.

تمام معرفهای فوق با سیستم کاملاً خودکار نمونه به جواب AIO 800 سازگار هستند، که باعث کاهش عملیات دستی و آلودگی متقاطع و بهبود کارایی و ایمنی زیستی میشود.
۴.۳ سناریوی ۳: نظارت ژنومی و تحلیل دودمان ویروسی
قابل اجرا برای آزمایشگاههای مرجع ملی، مؤسسات تحقیقاتی بهداشت عمومی، مطابق با موضع سازمان بهداشت جهانی در مورد NGS.
راهکارهای نظارت ژنومی Macro & Micro-Test از توالییابی کل ژنوم برای ردیابی ویروس، شفافسازی زنجیره انتقال، نظارت بر گونهها و تنظیم استراتژی واکسن پشتیبانی میکنند. آنها از گردشهای کاری دستی/خودکار پشتیبانی میکنند، توان عملیاتی و تکرارپذیری را بهبود میبخشند و آزمایشگاهها را قادر میسازند تا از آزمایشهای روتین به نظارت پیشرفته ارتقا یابند، که مطابق با تأکید سازمان بهداشت جهانی بر تقویت نظارت بر تکامل ویروسی است.

۴.۴ ارزش راهکارهای یکپارچه
ماکرو و میکرو-تست، راهکارهای تشخیصی کاملی برای تشخیص آربوویروس ارائه میدهد و از هر مرحله از مدیریت شیوع بیماری پشتیبانی میکند: ابزارهای غربالگری سریع برای مراکز مراقبتهای بهداشتی خط مقدم، تأیید مولکولی برای تشخیص دقیق و قابلیتهای تجزیه و تحلیل کل ژنوم برای نظارت اپیدمیولوژیک. این راهکارها با سنجشهای با کارایی بالا، گردشهای کاری انعطافپذیر و پلتفرمهای آماده برای اتوماسیون، آزمایشگاهها و سیستمهای بهداشت عمومی را قادر میسازند تا آمادگی و واکنش به تهدیدات نوظهور آربوویروسی را در سراسر جهان تقویت کنند.
منابع
[1] سازمان بهداشت جهانی. آزمایش آزمایشگاهی ویروس دنگی: راهنمای موقت، آوریل 2025. ژنو: سازمان بهداشت جهانی؛ 2025.
[2] گروه مشاوره فنی ابتکار جهانی آربوویروس سازمان بهداشت جهانی. تقویت آمادگی و پاسخ جهانی به تهدیدات بیماریهای آربوویروسی: فراخوانی برای اقدام. لنست اینفکت دیس. 2026؛26(1):15-17.
[3] میکروب لنست. غلبه بر معضل تشخیص تب دنگی. میکروب لنست. 2025;6(7):101190.
زمان ارسال: 20 مارس 2026
