۲۴ مارس ۲۰۲۶، سی و یکمین روز جهانی سل است. سازمان بهداشت جهانی (WHO) شعار جهانی امسال را ... اعلام کرده است.«بله! ما میتوانیم سل را ریشهکن کنیم!»با تأکید بر اینکه رهبری قوی دولت، تعهد سیاسی پایدار و اقدامات هماهنگ چندبخشی برای پایان دادن به همهگیری سل ضروری است.

پیشرفت جهانی و چالشهای باقیمانده
طبق گزارش جهانی سل ۲۰۲۵، کنترل جهانی سل در سال ۲۰۲۴ به نقطه عطف قابل توجهی دست یافت، به طوری که هم ...کاهش میزان ابتلا و مرگ و میربرای اولین بار از زمان همهگیری کووید-۱۹.
یک تخمین۱۰.۷ میلیون نفردر سال 2024 به سل مبتلا شدند، از جمله 54٪ مرد، 35٪ زن و 11٪ کودک و نوجوان. در میان این موارد، تقریباً۶۱۹۰۰۰ (۵.۸٪)همزمان به HIV مبتلا بودند، و۳۹۰،۰۰۰ (۳.۶٪)سل مقاوم به چند دارو یا مقاوم به ریفامپین (MDR/RR-TB) بودند.
سل تقریباً ایجاد میشود۱.۲۳ میلیون مرگدر سال 2024، همچنان عامل اصلی مرگ و میر ناشی از عفونت در سطح جهان است و از کووید-19 پیشی گرفته است. پس از سه سال افزایش بین سالهای 2021 تا 2023، میزان ابتلا به سل در جهان در سال 2024 تقریباً 2 درصد کاهش یافت که نشان دهنده بهبود تدریجی خدمات درمانی سل است.[1]
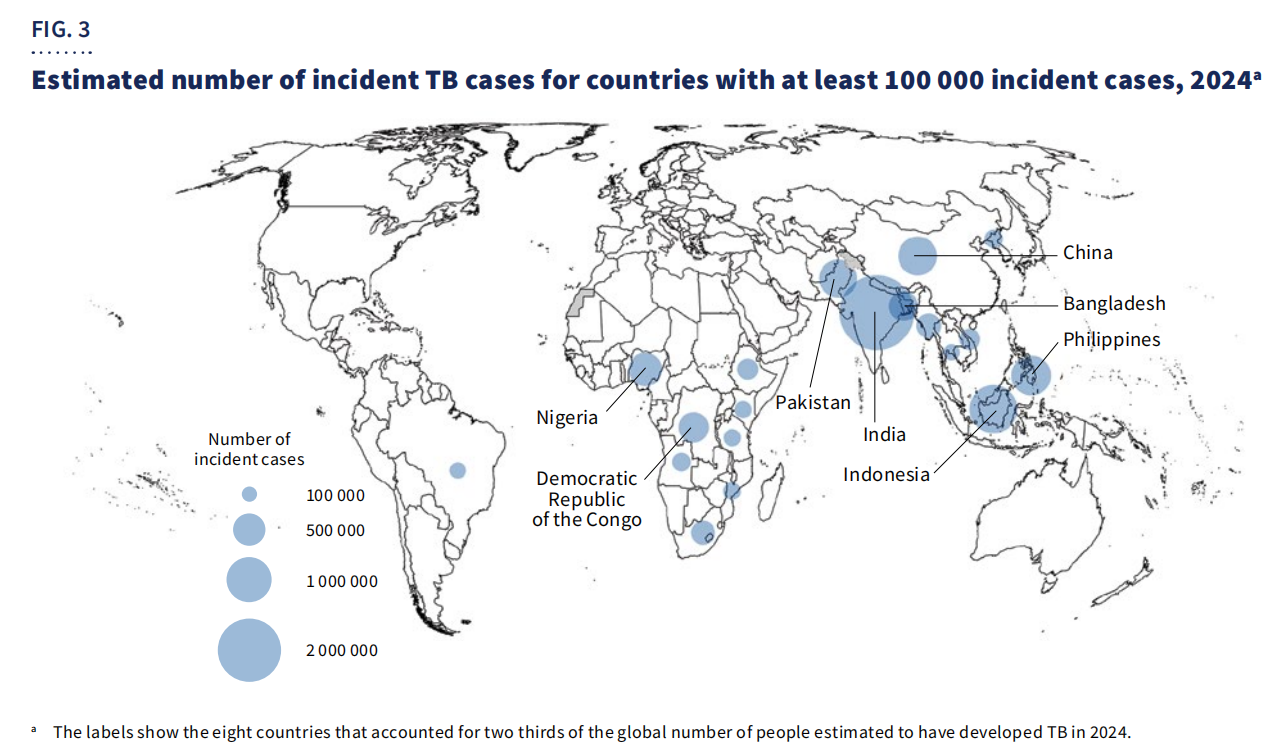
از نظر جغرافیایی،۶۷٪ موارداین موارد در هشت کشور متمرکز بودند: هند، اندونزی، فیلیپین، چین، پاکستان، نیجریه، جمهوری دموکراتیک کنگو و بنگلادش.
علیرغم پیشرفتها، سل همچنان یکی از علل اصلی مرگ و میر در میان افراد مبتلا به HIV و یکی از عوامل اصلی مرگ و میر مرتبط با مقاومت ضد میکروبی است. بودجه جهانی همچنان ناکافی است و تنها ...۵.۹ میلیارد دلار آمریکادر سال ۲۰۲۴ در دسترس خواهد بود—بسیار پایینتر ازهدف سالانه ۲۲ میلیارد دلار آمریکابرای سال 2027 تعیین شده است.
این ارقام، نیاز فوری به تقویت برنامههای کنترل سل در سطح جهانی، با تمرکز بر گسترش دسترسی به روشهای تشخیصی، بهبود نتایج درمان و پرداختن به عوامل اجتماعی مؤثر در انتقال سل را برجسته میکند. سل همچنان به همکاری قوی بینالمللی و تعهد سیاسی برای دستیابی به اهداف استراتژی پایان سل نیاز دارد.
مایکوباکتریوم توبرکلوزیس: پاتوژنز و طبقهبندی
مایکوباکتریوم توبرکلوزیس (MTB/M. tuberculosis) عامل اصلی و شایعترین پاتوژن مسئول بیماری سل (TB) است. این باکتری میتواند از طریق دستگاه تنفسی، دستگاه گوارش یا پوست و غشاهای مخاطی آسیبدیده وارد بدن انسان شود و اندامهای متعددی را آلوده کرده و باعث ایجاد اشکال مختلف سل شود. سل ریوی که عمدتاً از طریق قطرات منتقل میشود، بیش از 80٪ موارد سل را تشکیل میدهد. علائم رایج شامل سرفه، تولید خلط و خلط خونی است. پس از عفونت در ریهها، باکتری ممکن است از طریق جریان خون به سیستمهای متعدد گسترش یابد و به طور بالقوه منجر به سل اسکلتی، ادراری یا گوارشی شود.[2]
MTB بخشی از جنس مایکوباکتریوم است که شامل موارد زیر است:
- کمپلکس مایکوباکتریوم توبرکلوزیس (MTBC): شامل M. tuberculosis، M. bovis، M. africanum، M. canettii و M. microti و غیره. در حالی که M. tuberculosis عامل اصلی سل است، M. bovis و M. africanum نیز میتوانند باعث ایجاد این بیماری شوند.
- مایکوباکتریهای غیر سلی (NTM).
- مایکوباکتریوم لپره، عامل بیماری جذام.
رویکردهای تشخیصی آزمایشگاهی
تشخیص دقیق و به موقع برای کنترل مؤثر سل ضروری است. سازمان بهداشت جهانی تأکید میکند کهفناوریهای تشخیص مولکولی سریع، با فراهم کردن امکان شناسایی بسیار حساس و اختصاصی عوامل بیماریزا و همزمان تشخیص مقاومت دارویی، تشخیص سل را اساساً متحول کردهاند.[1].
- میکروسکوپ و کشتe: کشت همچنان استاندارد طلایی برای تشخیص سل است، زیرا امکان شناسایی قطعی ارگانیسمهای زنده را فراهم میکند و از آزمایش حساسیت دارویی و تجزیه و تحلیل ژنومی پشتیبانی میکند. با این حال، به دلیل سرعت رشد آهسته مایکوباکتریوم توبرکلوزیس، نتایج معمولاً به ۲ تا ۸ هفته زمان نیاز دارند که کاربرد بالینی آن را در تصمیمگیریهای فوری محدود میکند.
-آزمایش ایمونولوژیک: روشهای ایمونولوژیکی، از جمله آزمایش پوستی توبرکولین (TST) و سنجش آزادسازی اینترفرون گاما (IGRA)، پاسخهای ایمنی میزبان به عفونت سل را تشخیص میدهند. اگرچه این سنجشها برای شناسایی عفونت نهفته مفید هستند، اما نمیتوانند به طور قابل اعتمادی بین عفونت فعال و قبلی تمایز قائل شوند و بنابراین در شرایط با بار بالا، ویژگی تشخیصی محدودی دارند.
-تشخیص مولکولی (NAAT): آزمایشهای مبتنی بر DNA مانند تکثیر اسید نوکلئیک (NAAT) به دلیل حساسیت و اختصاصیت بالای آنها توصیه میشوند.
-توالییابی نسل بعدی هدفمند (tNGS): فناوریهای توالییابی هدفمند، شناسایی با وضوح بالا از جهشهای مرتبط با مقاومت را فراهم میکنند. دستورالعملهای سازمان بهداشت جهانی، tNGS را به عنوان ابزاری پیشرفته برای تشخیص مقاومت دارویی پس از تشخیص توصیه میکنند و از استراتژیهای درمانی دقیق پشتیبانی میکنند [3].
-توالییابی نسل بعدی متاژنومیک (mNGS): توالییابی متاژنومیک امکان تشخیص بیطرفانه طیف وسیعی از عوامل بیماریزا را بدون انتخاب هدف قبلی فراهم میکند. این رویکرد بهویژه در سناریوهای بالینی پیچیده یا نامشخص، از جمله عفونتهای مختلط و بیماران دارای نقص ایمنی، که در آنها تشخیصهای مرسوم ممکن است ناکافی باشند، ارزشمند است.
سازمان بهداشت جهانی (WHO) همچنین تأکید میکند که تأیید میکروبیولوژیکی برای شروع درمان مناسب و بهبود پیامدهای بیمار ضروری است و بر اهمیت ادغام تشخیصهای مولکولی پیشرفته در برنامههای کنترل سل تأکید میکند [1].
راهکارهای جامع تشخیص مولکولی از Macro & Micro-Test
۱.تشخیص PCR چندگانه برای سل و مقاومت داروییسل
| کد محصول | نام محصول | صدور گواهینامه |
| HWTS-RT001 | کیت تشخیص DNA مایکوباکتریوم توبرکلوزیس (PCR فلورسانس) | CE |
| HWTS-RT137 | کیت تشخیص جهش مقاومت به ایزونیازید در مایکوباکتریوم توبرکلوزیس (منحنی ذوب) | CE |
| HWTS-RT074 | کیت تشخیص مقاومت مایکوباکتریوم توبرکلوزیس به اسید نوکلئیک و ریفامپین (منحنی ذوب) | CE |
| HWTS-RT102 | کیت تشخیص اسید نوکلئیک بر اساس تکثیر ایزوترمال پروب آنزیمی (EPIA) برای مایکوباکتریوم توبرکلوزیس | CE |
| HWTS-RT144 | کیت تشخیص اسید نوکلئیک کمپلکس مایکوباکتریوم توبرکلوزیس خشک شده به روش انجمادی (تکثیر ایزوترمال با پروب آنزیمی) | CE |
| HWTS-RT105 | کیت تشخیص DNA مایکوباکتریوم توبرکلوزیس خشک شده با روش انجمادی (PCR فلورسانس) | CE |
| HWTS-RT147 | کیت تشخیص مقاومت به ایزونیازید و اسید نوکلئیک مایکوباکتریوم توبرکلوزیس (منحنی ذوب) | CE |
وقتی سوءظن بالینی قوی به سل (TB) وجود داشته باشد،HWTS-RT147این آزمایش برای تشخیص کیفی عفونت MTB و سل مقاوم به چند دارو (MDR-TB) توصیه میشود. این آزمایش جهشها را درژن rpoBکه منجر به مقاومت به ریفامپین (RIF) و جهش درژنهای katG و InhAکه با مقاومت به ایزونیازید (INH) مرتبط هستند. این روش، آزمایشی کارآمد و یکباره برای MTB و MDR-TB ارائه میدهد که شامل کنترل کیفیت داخلی برای به حداقل رساندن نتایج منفی کاذب و تضمین نتایج سریع و دقیق است.
۲.توالییابی هدفمند PTNseq برای پاتوژنهای تنفسی و تعیین پروفایل مقاومت
| کد محصول | نام محصول | مشخصات |
| HWKF-TS0001 | کیت غنیسازی ژن پاتوژن عفونت جریان خون PTNseq | ۲۴ تست/کیت |
| HWKF-TS0002 | کیت غنیسازی ژن میکروارگانیسمهای بیماریزای عفونت سیستم عصبی مرکزی PTNseq | ۲۴ تست/کیت |
| HWKF-TS0003 | کیت غنیسازی ژن پاتوژن عفونت تنفسی PTNseq | ۲۴ تست/کیت |
| HWKF-AT0003 | کیت ساخت کتابخانه غنیسازی خودکار میکروارگانیسمهای بیماریزای عفونت تنفسی PTNseq (ONT) | ۲۴ تست/کیت |
| HWKF-TS0004 | کیت غنیسازی ژن پاتوژنهای عفونی طیف گسترده PTNseq | ۲۴ تست/کیت |
| HWKF-TS0005 | کیت غنیسازی ژن میکروارگانیسمهای بیماریزای عفونی با طیف وسیع PTNseq | ۲۴ تست/کیت |
| HWKF-TS0151 | کیت غنیسازی ژنهای تایپینگ مایکوباکتریوم و مقاومت دارویی (روش تکثیر چندگانه) | ۲۴ تست/کیت |
در موارد عفونتهای تنفسی مختلط (شامل عفونتهای دستگاه تنفسی فوقانی و تحتانی، سل و بیماریهای مزمن تنفسی) یا هنگامی که تجزیه و تحلیل ژن مقاومت دارویی مورد نیاز است (مثلاً سل مشکوک به مقاومت دارویی)،سری PTNseq از تشخیص ژن هدفمند با توان عملیاتی بالابر اساس فناوری پیشرفته توالییابی هدفمند، PTNseq از PCR چندگانه فوق العاده برای غنیسازی توالیهای هدف خاص، همراه با توالییابی با توان عملیاتی بالا و فناوری نانوحفره نسل سوم برای شناسایی جامع پاتوژن و پروفایل مقاومت دارویی استفاده میکند.
این سیستم از پرایمرهای ثبتشده و با اختصاصیت بالا برای تکثیر فوق چندگانه ژنهای هدف استفاده میکند. این سیستم که توسط یک پایگاه داده اختصاصی و الگوریتمهای هوشمند بیوانفورماتیک پشتیبانی میشود، شناسایی دقیق پاتوژن را به همراه تجزیه و تحلیل ژنهای مقاومت دارویی و حدت ارائه میدهد. غنیسازی هدفمند، تداخل ناشی از DNA میزبان را کاهش میدهد، حساسیت را در نمونههایی با پیشینه انسانی بالا بهبود میبخشد و امکان تشخیص مؤثر اهداف دشوار مانندمایکوباکتریوم توبرکلوزیس، قارچها، باکتریهای درون سلولی، ویروسهای RNA و ژنهای مقاومت یا بیماریزایی.
PTNseq به حد تشخیص مشخصی دست مییابدتا 100 کپی در میلی لیترو پوششها۱۷۵ پاتوژن تنفسی رایج، شامل ۷۶ باکتری، ۷۳ ویروس، ۱۹ قارچ، ۷ مایکوپلاسما، و همچنینکلامیدیا, ریکتزیاو ۵۴ ژن مقاومت داروییاین پنل شامل موارد زیر است:مایکوباکتریوم توبرکلوزیسمایکوباکتریهای غیر سلی پیچیده و اصلی.
سری PTNseq حساسیت بالا را با مقرون به صرفه بودن ترکیب میکند، نرخ تشخیص پاتوژن را بهبود میبخشد و از درمان ضدمیکروبی فردی پشتیبانی میکند و در عین حال به کاهش مقاومت ضدمیکروبی کمک میکند. این سیستم که با سیستم آمادهسازی کتابخانه توالییابی ژنی کاملاً خودکار (AIOS) ادغام شده است، یک راهحل ساده و درون بیمارستانی را با زمان چرخش به سرعت ۶.۵ ساعت از نمونه تا نتیجه ارائه میدهد.

۳. توالییابی متاژنومیک برای تشخیص پاتوژنهای طیف گسترده
| کد محصول | نام محصول | مشخصات |
| HWKF-MN0011 | کیت تشخیص پاتوژن متاژنومیک (DNA-Illumina) | ۲۴ تست/کیت |
| HWKF-MN0018 | کیت تشخیص پاتوژن متاژنومیک (DNA-MGI) | ۲۴ تست/کیت |
| HWKF-MN0021 | کیت تشخیص پاتوژن متاژنومیک (DNA-ONT) | ۲۴ تست/کیت |
| HWKF-MN0012 | کیت تشخیص پاتوژن متاژنومیک (RNA-Illumina) | ۲۴ تست/کیت |
| HWKF-MN0019 | کیت تشخیص پاتوژن متاژنومیک (RNA-MGI) | ۲۴ تست/کیت |
| HWKF-MN0022 | کیت تشخیص پاتوژن متاژنومیک (RNA-ONT) | ۲۴ تست/کیت |
| HWKF-MN0013 | کیت تشخیص پاتوژن متاژنومیک (DNA+RNA-Illumina) | ۲۴ تست/کیت |
| HWKF-AYM0013 | کیت ساخت کتابخانه خودکار تشخیص پاتوژن متاژنومیک (DNA+RNA-Illumina) | ۲۴ تست/کیت |
| HWKF-MN0020 | کیت تشخیص پاتوژن متاژنومیک (DNA+RNA-MGI) | ۲۴ تست/کیت |
| HWKF-MN0023 | کیت تشخیص پاتوژن متاژنومیک (DNA+RNA-ONT) | ۲۴ تست/کیت |
وقتی تشخیص بالینی نامشخص است،تشخیص ژن با توان عملیاتی بالا در پاتوژن mNGSمیتوان آن را روی نمونههای مختلف بیمار، از جمله مایع لاواژ برونکوآلوئولار، خلط، سواب گلو، خون، پلورال افیوژن، چرک و نمونههای بافت انجام داد. این رویکرد از فناوری توالییابی متاژنومیک استفاده میکند، که در آن نمونههای مختلف تحت پیشتیمار هدفمند قرار میگیرند و به دنبال آن استخراج اسید نوکلئیک با استفاده از دانههای شیشهای و آنزیمهای هضمکننده دیواره انجام میشود و راندمان استخراج را افزایش میدهد. توالییابی با پلتفرمهای متعدد سازگار است و حجم بالای دادهها را برای بهبود حساسیت mNGS و یکپارچگی مونتاژ تضمین میکند. دادهها با استفاده از یک پایگاه داده خودساخته و الگوریتمهای هوشمند برای تشخیص تجزیه و تحلیل میشوند.بیش از ۲۰،۰۰۰ عامل بیماریزاشامل باکتریها، قارچها، ویروسها و انگلها، که اطلاعاتی در مورد میکروارگانیسمهای بیماریزای مشکوک ارائه میدهد. این روش برای بیماران با تشخیص دشوار، بدحال یا دارای نقص ایمنی، از جمله شناسایی موارد زیر، مناسب است:ام تی بیپیچیدهوان تی امو همچنین عفونتهای مختلط. این روش به طور قابل توجهی میزان تشخیص پاتوژن را بهبود میبخشد و به هدایت استفاده بالینی هدفمند از آنتیبیوتیک کمک میکند و تشخیص دقیق عفونت را ممکن میسازد.
نتیجهگیری
اگرچه پیشرفتهای قابل توجهی حاصل شده است، اما سل همچنان یک چالش بزرگ سلامت جهانی است، به ویژه در زمینه مقاومت دارویی، شکافهای بودجهای و دسترسی نابرابر به تشخیص.
سازمان بهداشت جهانی تأکید میکند که افزایش دسترسی به تشخیصهای مولکولی سریع و فناوریهای پیشرفته تعیین توالی برای دستیابی به اهداف استراتژی پایان سل ضروری است. با نوآوری، سرمایهگذاری و همکاری جهانی مداوم، پایان دادن به سل دیگر یک آرزو نیست، بلکه یک هدف قابل دستیابی است.
منابع:
- سازمان بهداشت جهانی. گزارش جهانی سل 2024/2025: آزمایش تشخیصی و درمان.
- سازمان بهداشت جهانی. راهنمای WHO برای انتخاب آزمایشهای مولکولی تشخیصی سریع توصیهشده توسط WHO برای تشخیص سل و سل مقاوم به دارو.
- سازمان بهداشت جهانی. دستورالعملهای تلفیقی سازمان بهداشت جهانی در مورد سل: بخش ۳ - تشخیص (بهروزرسانی ۲۰۲۴).
زمان ارسال: 24 مارس 2026
