I. بررسی اجمالیاسمودستورالعمل ۲۰۲۵
در آگوست 2025، ESMO رسماً «سرطان ریه سلول غیرکوچک اولیه و محلی پیشرفته: راهنمای بالینی ESMO برای تشخیص، درمان و پیگیری» را منتشر کرد که در مجله برتر انکولوژی Annals of Oncology منتشر شد. این اولین بهروزرسانی جامع از زمان نسخه 2017 است و مرجعی بسیار معتبر برای انکولوژیستها در سراسر جهان فراهم میکند.

سرطان ریه بالاترین میزان بروز و مرگ و میر را در بین تمام بدخیمیها در سطح جهان دارد. هر ساله بیش از ۲.۲ میلیون مورد جدید و بیش از ۱.۸ میلیون مرگ و میر رخ میدهد که سرطان ریه را به علت اصلی مرگ و میر ناشی از سرطان در مردان و زنان تبدیل میکند. سرطان ریه سلول غیرکوچک (NSCLC) تقریباً ۸۰ تا ۸۵ درصد از کل بیماران مبتلا به سرطان ریه را تشکیل میدهد. در برابر این پیشینه جدی، انتشار دستورالعمل ۲۰۲۵، حرکت علمی جدیدی را به عرصه بالینی وارد میکند و بهروزرسانی استراتژیهای آزمایش نشانگرهای زیستی به ویژه حیاتی است.
دوم. تفسیر بهروزرسانیهای کلیدی دستورالعملها
۲.۱ آزمایش نشانگرهای زیستی: از «اختیاری» تا «ضروری»
دستورالعمل ۲۰۲۵ یک تغییر استراتژیک مهم در مورد آزمایش نشانگرهای زیستی ایجاد میکند. این دستورالعمل به صراحت بیان میکند که آزمایش نشانگرهای زیستی برای تصمیمگیری در مورد درمان در بیماران مبتلا به NSCLC مرحله IB-III ضروری است.
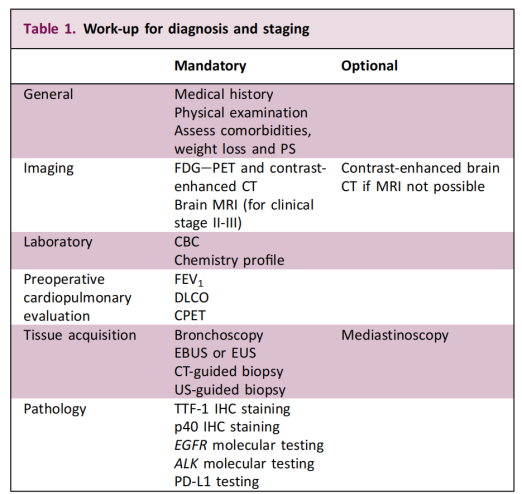
این توصیه، آزمایشهای مولکولی را از تمرکز قبلی خود بر بیماران مبتلا به بیماری پیشرفته به موارد قابل برداشت در مراحل اولیه گسترش میدهد. هدف اصلی، شناسایی جهشهای ژن محرک و ارائه مبنای علمی برای درمان دقیق شخصیسازی شده است. این دستورالعمل همچنین تأکید میکند که امکانسنجی بیوپسی و رویکرد تشخیصی باید توسط یک تیم چند رشتهای بر اساس ویژگیهای بیمار و تومور تعیین شود.
در مورد استراتژی خاص آزمایش، این دستورالعمل به وضوح توصیه میکند که آزمایش ژنتیکی قبل از تصمیمگیری جراحی انجام شود و حداقل باید EGFR و ALK را پوشش دهد. این مفهوم «آزمایش از قبل» اهمیت بالینی عمیقی برای طبقهبندی دقیق و درمان شخصیسازیشده NSCLC در مراحل اولیه دارد - بهموقع بودن و دقت نتایج آزمایش مستقیماً انتخاب درمان کمکی بعدی را تعیین میکند.
۲.۲ پیشرفتهای درمانی در سرطان ریه غیرکوچک (NSCLC) در مراحل اولیه با ژن محرک-آنکوژن مثبت
دستورالعمل ۲۰۲۵، شواهد حاصل از چندین مطالعه بالینی بزرگ را ادغام میکند تا یک مسیر درمانی دقیق و روشن برای بیماران مبتلا به NSCLC در مراحل اولیه با ژن محرک-آنکوژن مثبت ایجاد کند.
بیماران مثبت با جهش EGFR:بر اساس کارآزمایی برجسته ADAURA، داروی کمکی اوسیمرتینیب پس از عمل به مدت سه سال به استاندارد جهانی مراقبت از بیماران مبتلا به حذف اگزون ۱۹ EGFR یا جهشهای L858R در اگزون ۲۱ تبدیل شده است. کارآزمایی ADAURA یک مطالعه فاز III بینالمللی، چند مرکزی، تصادفی و کنترلشده است که اثربخشی و ایمنی داروی کمکی اوسیمرتینیب را در بیماران مبتلا به NSCLC جهشیافته EGFR مرحله IB-IIIA که کاملاً برداشته شدهاند، ارزیابی میکند. این مطالعه نشان داد که اوسیمرتینیب به طور قابل توجهی بقای بدون بیماری و بقای کلی را در مقایسه با دارونما بهبود میبخشد و اوسیمرتینیب را به عنوان استاندارد جدید مراقبت برای این جمعیت معرفی میکند. با این حال، تجزیه و تحلیلهای اکتشافی کارآزمایی ADAURA نشان داد که تقریباً ۳۶٪ از قطع درمان زودهنگام به دلیل عوارض جانبی و ۳۱٪ دیگر به دلیل تصمیم بیمار بوده است. این یافته بر نیاز به آزمایش دقیق پایه قبل از درمان تأکید میکند تا اطمینان حاصل شود که درمان هدفمند به بیمارانی داده میشود که میتوانند از مزایای پایدار بهرهمند شوند.
بیماران ALK مثبت:بر اساس کارآزمایی ALINA، اَلکتینیب کمکی پس از عمل به مدت دو سال، اکنون استاندارد مراقبت است. در تجزیه و تحلیل اولیه کارآزمایی تصادفی فاز III با برچسب باز ALINA، اَلکتینیب مزیت بقای بدون بیماری قابل توجهی را در جمعیت مرحله II-IIIA با نسبت خطر 0.24 نشان داد. دادههای بهروز شده از کارآزمایی ALINA که در کنگره ESMO 2025 ارائه شد، نشان داد که پس از ≥3 سال پیگیری، مزیت DFS اَلکتینیب "پایدار و از نظر بالینی معنادار" باقی ماند، با نسبت خطر 0.36 در جمعیت مرحله II-IIIA. آخرین میزان بقای کلی 4 ساله گزارش شده به 98.4٪ رسید، میزان DFS 4 ساله 75.5٪ بود و DFS سیستم عصبی مرکزی نیز بهبود یافت، بدون هیچ سیگنال ایمنی جدیدی. این دادههای قوی، اَلکتینیب کمکی را به عنوان استاندارد مراقبت پس از برداشتن NSCLC مثبت ALK بیشتر تثبیت میکنند و بر ارزش آزمایش دقیق برای شناسایی چنین بیمارانی تأکید میکنند.
انتخاب روش آزمایش:دستورالعمل ESMO 2025 به صراحت فهرست میکندسنجشهای پانلی RT-PCR چندگانهدر کنار NGS مبتنی بر RNA، IHC و FISH به عنوان یکی از رویکردهای فنی توصیه شده برای تشخیص ادغام ALK. این نشان میدهد که الزام اصلی این دستورالعمل، انجام آزمایش برای هدایت تصمیمات بالینی است، نه الزام به یک پلتفرم آزمایش خاص. برای محصولات RT-PCR که بر تشخیص EGFR و ALK متمرکز هستند، این استراتژی آزمایش انعطافپذیر، توجیه قوی مبتنی بر دستورالعمل را برای استفاده از آنها در عمل بالینی فراهم میکند.
III. راهکارهای فنی تست دقیق
دستورالعمل ۲۰۲۵، آزمایش را به مرحله تصمیمگیری قبل از جراحی منتقل میکند که این امر، دقت، حساسیت و دسترسیپذیری سنجش را افزایش میدهد. دو محصول تشخیصی مبتنی بر RT-PCR که در زیر توضیح داده شدهاند، از نظر فنی دقیقاً با الزامات دستورالعمل مطابقت دارند.
۳.۱ کیت تشخیص جهش EGFR – پلتفرم فناوری ARMS پیشرفته
فناوری هستهایفناوری پیشرفته ARMS امکان تکثیر اختصاصی توالیهای جهشیافته با فراوانی کم را در برابر پسزمینهای با فراوانی بالای توالیهای وحشی فراهم میکند.
سه اقدام حفاظتی فنی:
ARMS بهبود یافته → تشخیص جهش را بهبود میبخشد
غنیسازی آنزیمی → توالیهای وحشی را هضم و توالیهای جهشیافته را غنی میکند
- مسدود کردن دما → تکثیر غیر اختصاصی را سرکوب میکند
عملکرد: حساسیتفراوانی آلل جهشیافته ۱٪
کنترل آلودگیکنترل داخلی داخلی + آنزیم UNG از آلودگی جلوگیری میکند
زمان تحویل: عملکرد لوله بسته، تقریباً۱۲۰ دقیقه
سازگاری نمونه:بافت/بیوپسی مایعنمونهها → به الزامات «آزمایش از قبل» میپردازد
پوشش:۴۵ جهشدر اگزونهای ۱۸ تا ۲۱ EGFR، دقیقاً مطابق با نواحی هایلایت شده در دستورالعمل (حذفهای اگزون ۱۹ و اگزون ۲۱ L858R)
استفاده بالینی: مستقیماً درمان EGFR-TKI را هدایت میکند
۳.۲ کیت تشخیص فیوژن MMT EML4-ALK – راهکار تشخیص فیوژن مبتنی بر RNA

-پلتفرم فناوریRT-PCR مبتنی بر RNA - مزایای ذاتی نسبت به روشهای مبتنی بر DNA برای تشخیص فیوژن ارائه میدهد
-مزیت مبتنی بر RNA: رونوشتهای ترکیبی بیانشده را مستقیماً تشخیص میدهد و به طور مؤثر از نتایج منفی کاذب جلوگیری میکند.
-شواهد مطالعهدر همجوشیهای ALK با فراوانی کم، RT-PCR به طور قابل توجهی قابل اعتمادتر از آزمایشهای مبتنی بر DNA است.
-حساسیت: تشخیص فیوژنها تا۲۰ نسخه برای هر واکنش
-پوشش انواع: پوششها۱۲ نوع رایج فیوژن EML4-ALK(شامل گونه ۱ حدود ۳۳٪؛ گونههای ۳a/3b با هم حدود ۲۹٪)
-عملیات و کنترل آلودگیلوله بسته، تقریباً ۱۲۰ دقیقه؛ کنترلهای فرآیند داخلی + آنزیم UNG از نتایج کاذب جلوگیری میکند
-سازگاری با ابزارسازگار با انواع ابزارهای PCR بلادرنگ رایج
-ترازبندی راهنما: کاملاً مطابق با دستورالعمل ESMO
IV. تطابق بین سنجشها و توصیههای راهنما
این دو محصول تشخیصی در ابعاد کلیدی زیر با دستورالعمل ESMO 2025 سرطان ریه غیر سلول کوچک زودرس و پیشرفته موضعی بسیار سازگار هستند:
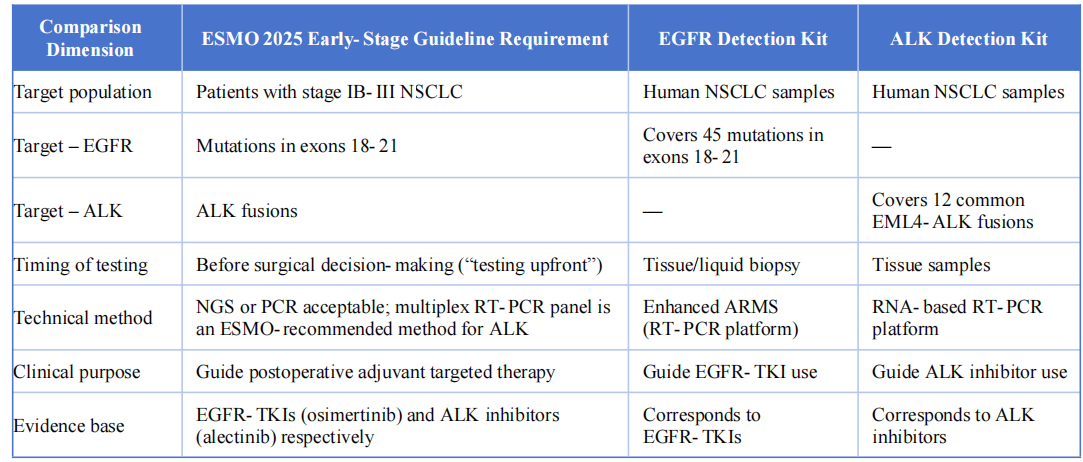
نتیجه گیری
دستورالعمل ESMO 2025 برای سرطان ریه غیرکوچک (NSCLC) در مراحل اولیه، عصر جدیدی از تشخیص و درمان دقیق را با محوریت «آزمایش اولیه، هدفگیری دقیق و بهینهسازی درمان.کیت تشخیص جهش EGFR و کیت تشخیص فیوژن MMT EML4-ALK از طریق مسیرهای فنی متمایز، الزامات دستورالعمل را برای اهداف، زمانبندی و دقت برآورده میکنند.
کیت EGFR از فناوری ARMS پیشرفته برای تشخیص با حساسیت بالا جهشهای هدفمند در نمونههای محدود استفاده میکند و از بیوپسی بافت و مایع برای امکانپذیر کردن «آزمایش اولیه» پشتیبانی میکند.
کیت ALK مبتنی بر RT-PCR مبتنی بر RNA است که مزایایی نسبت به روشهای DNA برای تشخیص فیوژن ارائه میدهد و با توصیه ESMO مبنی بر پانلهای RT-PCR چندگانه برای آزمایش ALK مطابقت دارد.
این دو محصول در کنار هم، یک راهکار آزمایش دقیق مطابق با دستورالعمل ESMO 2025 را تشکیل میدهند که از درمان کمکی شخصیسازیشده برای NSCLC در مراحل اولیه پشتیبانی میکند.
مراجع:
- زر ای، آن ام جی، بارلسی اف و همکاران. سرطان ریه غیرسلول کوچک زودرس و موضعی پیشرفته: راهنمای بالینی ESMO برای تشخیص، درمان و پیگیری. مجله آن کول. 2025؛ 36(11): 1245-1262. doi:10.1016/j.annonc.2025.08.003
زمان ارسال: مه-06-2026

